- JST トップ
- /
- 戦略的創造研究推進事業
- /
 ERATO
ERATO- /
- 研究領域の紹介/
- 終了領域/
- 橋本光エネルギー変換システムプロジェクト
橋本光エネルギー変換システムプロジェクト

研究総括 橋本 和仁
(東京大学 大学院工学系研究科 教授)
研究期間:2006年~2012年
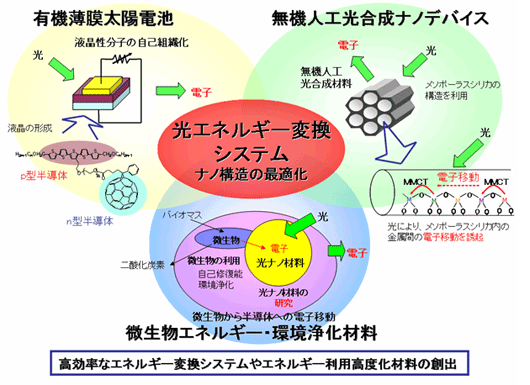
「最先端の基礎化学の成果を利用することにより、新たなエネルギー変換技術(特に太陽エネルギー)を開発し、人類・社会に貢献する」の目標のもとで、希少金属などを使用せず自然界にありふれた安全・安価な材料(有機物質や、酸化鉄・硫化鉄などの鉄化合物、さらに微生物)でエネルギー獲得を行うという考え方で、以下の研究を進めてきました。
有機薄膜太陽電池では、より高い太陽光エネルギー変換効率を実現させるため、50以上の光学的バンドギャップの狭い新規ポリマー設計・合成を進め、2010年には、太陽光照射下における短絡電流密度が23.7 mA/cm2という、既報告中では最高値を示すポリマーの開発に成功しました。
人工光合成の開発においては、Mn系酸素発生触媒の高活性化にも取り組み、世界で最初にMn系触媒を介した水の酸化反応の中間体検出に成功し、過電圧の低下が切望されている酸素発生触媒に対して明確な設計指針を与える成果を得ました。
微生物燃料電池おいては、遺伝子工学的手法により電流生産量が野生株よりも50%高い変異株の作成に成功し、また電極表面をカーボンナノチューブなどで被覆することにより、出力密度が従来の5倍以上も増加するという結果が得られました。
研究成果集
有機高分子材料グループ
有機薄膜太陽電池の研究を行い、分子設計からのアプローチにより、共役系ブロックコポリマーの相分離構造を用いて太陽電池に理想的な構造を自発的に形成させることに成功した。また、低い表面エネルギーを持つ新規なフラーレン化合物(F-PCBM)を混合バルクヘテロ接合の溶液に少量混入させることで、バッファ相として機能するF-PCBM層が自発的に形成され、太陽電池特性が顕著に向上することも見出した。これらの成果は大面積太陽電池を簡単な塗布プロセスで作成するための基礎技術として期待される。
また、より高い太陽光エネルギー変換効率を実現させるため、光学的バンドギャップの狭いポリマーの設計・合成を行い、これまで50以上の新規ポリマー群を報告した。これらの半導体ポリマーをフラーレン誘導体と組み合わせることで、より高い開放電圧を与えるポリマーや、近赤外領域に大きな吸収をもち、1100 nmの波長まで光電変換できるポリマーを開発することに成功した。2010年には、太陽光照射下における短絡電流密度が23.7 mA/cm2という、既報告中で最高値のポリマーの開発に成功した。
フラーレンを使わない全ポリマー型有機薄膜太陽電池においても、太陽光エネルギー変換効率2.2 % という世界最高のものを得ることに成功した。さらに変換効率4%を超えるものが得られており、研究を展開している。また、フッ素化した有機半導体の自発的な表面配置と、有機薄膜の貼り合わせ技術を組み合わせることで、有機薄膜太陽電池の界面構造を制御できることを示した。
- Y. Zhang, K. Tajima, K. Hirota, K. Hashimoto, J. Am. Chem. Soc., 2008, 130 (25), 7812-7813.
- S. Miyanishi, Y. Zhang, K. Tajima, K. Hashimoto, Chem. Commun., 2010, 46, 6723-6725.
- E. Zhou, J. Cong, K. Hashimoto, K. Tajima, Energy Environ. Sci., 2012, 5, 9756-9759.
- A. Tada, Y.F. Geng, Q.S. Wei, K. Hashimoto, K. Tajima, Nature Mater., 2011, 10, 450.
金属錯体グループ
人工光合成系の開発において、炭酸ガスの固定化に向けた多核金属クラスターでの多電子移動を駆動するナノデバイスに向けた研究を進め、多核系・光誘起電荷移動錯体(Ce/PW12O40)の構築に成功した。また、Mn系酸素発生触媒の高活性化にも取り組み、世界で最初にMn系触媒を介した水の酸化反応の中間体検出に成功し、過電圧の低下が切望されている酸素発生触媒に対して明確な設計指針を与えた。さらに、この設計指針を基に、酸化マンガン表面に窒素を含む高分子を配位した触媒を調整し、中性領域で極めて酸素発生加電圧の低い触媒を得ることに成功した。
一方、微生物グループとの交流から、酸化鉄上に生息する微生物系内に酸化鉄ナノコロイドを加えることで、微生物が好む生育環境が自己組織化的に系内に構築されることを見出し、微生物産生電流を50倍以上に増大させることに成功した。この飛躍的な電流増加は、酸化鉄ナノコロイドが媒介して電流発生微生物が自己集合し、これにより長距離電子伝達系が形成されたためであることが明らかになった。この結果は、微生物燃料電池の格段の性能向上につながる可能性を持つ。
また、微生物からの細胞外電子伝達が外膜にある金属錯体分子(シトクロームc)を経由する進行メカニズムについての分光電気化学、光ピンセットを用いた単一微生物細胞の電気化学などの成果を報告した。さらに生きた微生物の電子移動ダイナミックスや微生物呼吸経路の電気化学的スイッチング、微生物間の相互情報伝達による細胞外電子伝達制御など基礎学問として高いレベルの成果が得られており、今後、エネルギーデバイス開発へのフィードバックも期待できる。
炭素をベースとした新規酸素還元触媒開発においては、出発原料として電気伝導特性に優れたグラフェンを利用することで、鉄と窒素のドーピングに要する熱処理時間を極短時間に抑え、これによって高活性・高安定性の酸素還元触媒を合成することに成功した。また、窒素含有量の非常に高い高分子から作製した炭素系材料に鉄とコバルトを配位させて高活性・高安定性の酸素還元触媒を合成し、それを用いた微生物燃料電池において白金触媒系の2倍以上の電力生産を得ることに成功した。
- T. Takashima, K. Hashimoto, R. Nakamura, J. Am. Chem. Soc., 2012, 134, 18153-18156.
- T. Takashima, K. Hashimoto, R. Nakamura, J. Am. Chem. Soc., 2012, 134, 1519-1527
- R. Nakamura, F. Kai, A. Okamoto, G. J. Newton, K. Hashimoto, Angew. Chem. Int. Ed. 2009, 48, 508-511
- H. Liu , G J. Newton, R. Nakamura, K. Hashimoto, S. Nakanishi, Angew. Chem. Int. Ed., 2010, 49 (37), 6596-6566
- K. Kamiya, K. Hashimoto, S. Nakanishi, Chem. Commun., 2012, 48, 10213-10215
微生物グループ
微生物燃料電池の研究において、i) ゲノム情報をベースにした電流生産(細胞外電子伝達)機構の解明に関する論文を報告するとともに、ii)遺伝子工学的手法により電流生産量が野生株よりも50%高い変異株を作成することに成功した。
一方、電極表面にナノ構造の導入を試み、カーボンナノチューブなどで電極表面を被覆することにより、微生物燃料電池の出力密度は5倍以上も増加するという結果を得た。また、金属錯体グループで得られた酸化鉄ナノコロイドを微生物系に導入することにより電流密度が増大するとの知見について、燃料電池を構成する電流生産微生物群集系においても成立することを確認した。
また、自然環境中で生息する微生物がなぜ人工的な電極に電気を流すのかについても実証を試みた。酢酸と硝酸をそれぞれ電子供与体と電子受容体として、土壌細菌の代表株であるゲオバクターとチオバチルスとを共培養し、この培養系に導電性酸化鉄微粒子を添加したところ、それぞれ単独の菌では起こらない酢酸酸化に伴う硝酸還元が観測された。微生物が導電性ミネラルを電線として電子をやり取りし、お互いに助け合って生きていること(“電気共生”)の証明と考えられる。
カセット電極式微生物燃料電池を用いたモデル下水の処理実験では、水の滞留時間12時間程度でCOD除去率80%以上の良好な処理を達成した。
微生物太陽電池の研究では、「光合成真核藻類と従属栄養細菌の層状構造が電極表面に自己組織化されることにより光電流が得られる。」ことを見出した。この微生物群集の自己組織化を用いた系の光電変換効率は0.03%と低いものであったが、この知見を基に、光合成微生物と電流産生細菌の二種類のみを含んだ最少モデル共生系を構築したところ、光電変換効率は0.17%にまで上昇した。さらにこの考えを植物と電流生成微生物を用いた光電変換へと拡張し、水田を用い、イネの根圏に負極を、水中に正極を設置したところ、日中は発電量が上昇し、夜は低下することが示された。発電効率は約30 mW/m2と低いが、自然界をそのまま太陽電池として使える可能性を世界で初めて示した。
- G. J. Newton, S. Mori, R. Nakamura, K. Hashimoto, K. Watanabe, Appl. Envir. Microbiol., 2009, 75, 7674-7681
- K. Nishio, K. Hashimoto, K. Watanabe, Appl. Microbiol. Biotechnol., 2010, 86, 957-964
- K. Watanabe, M. Miyahara, T. Shimoyama, K. Hashimoto, Appl. Microbiol. Biotechnol., 2011, 92, 1307-1314
- S. Kato, K. Watanabe, K. Hashimoto, Proc. Nat. Acad. Sci. USA, 2012, 109, 10042-10049
- Y. Zhao, K. Watanabe, K. Hashimoto, J. Am. Chem. Soc., 2012, 134, 19528−19531












